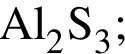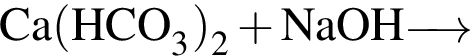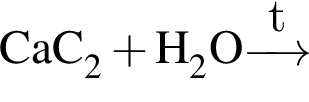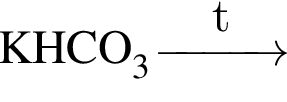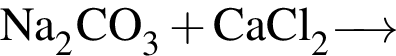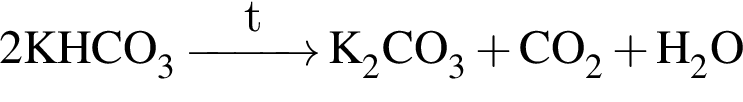Выберите верные утверждения:
1) температура кипения  ниже, чем
ниже, чем 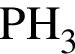 ;
;
2) валентность азота в 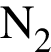 равна его степени окисления;
равна его степени окисления;
3) при увеличении давления (путём уменьшения объёма системы) равновесие реакции синтеза аммиака из простых веществ смещается в сторону продукта реакции;
4) валентность азота в хлориде аммония равна IV, а степень окисления равна -3;
5) при взаимодействии с магнием азот выступает в роли восстановителя;
6) в отличие от азота для фосфора характерна валентность V.
Ответ запишите в виде последовательности цифр в порядке возрастания, например: 123.
![]() ;
;![]() ;
;
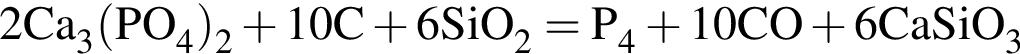
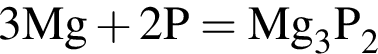 ;
; 
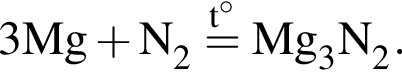 Так степень окисления азота в процессе реакции изменяется от 0 до -3, то он выступает в роли окислителя;
Так степень окисления азота в процессе реакции изменяется от 0 до -3, то он выступает в роли окислителя;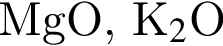
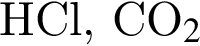
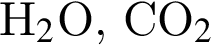
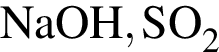
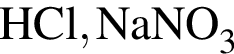
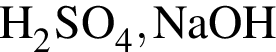
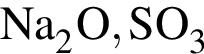
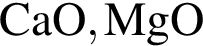
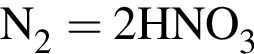
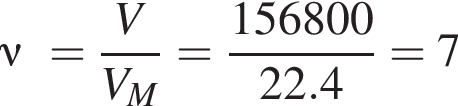 кмоль
кмоль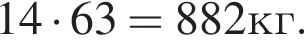
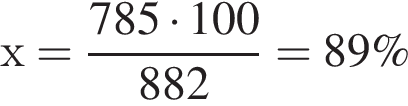
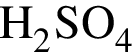 16% прибавили раствор иодида бария массой 100 г. При этом массовая доля серной кислоты растворе уменьшилась до 9%. Рассчитайте массовую долю (%)
16% прибавили раствор иодида бария массой 100 г. При этом массовая доля серной кислоты растворе уменьшилась до 9%. Рассчитайте массовую долю (%) 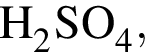
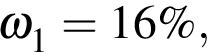
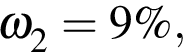 100 г.
100 г. 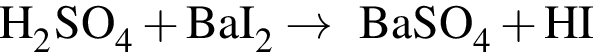
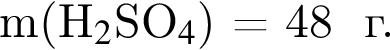
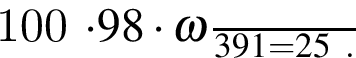
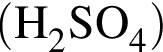
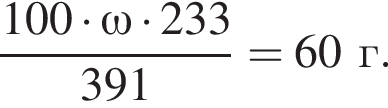
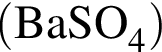
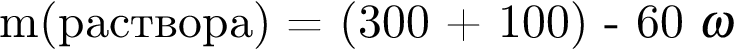
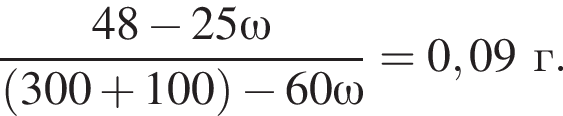

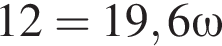
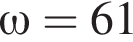
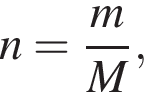 где n — число молей, m — масса вещества, M — молярная масса данного вещества, находим массу фосфора в 100 г аммофоса:
где n — число молей, m — масса вещества, M — молярная масса данного вещества, находим массу фосфора в 100 г аммофоса: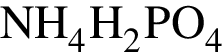 ) = 115x г.
) = 115x г.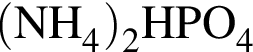 ) = 132y г.
) = 132y г.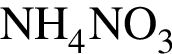 ) = (87,5 − 73) · 80/28 = 41 г.
) = (87,5 − 73) · 80/28 = 41 г.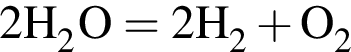
 кмоль
кмоль
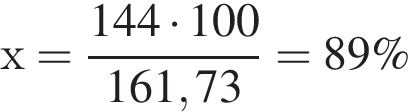

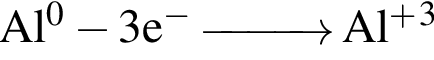
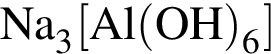 )=1476 г/246 г/моль=6 моль
)=1476 г/246 г/моль=6 моль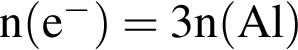 =18 моль
=18 моль
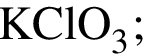
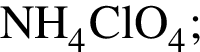
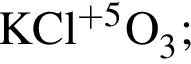
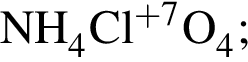
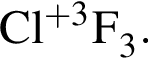
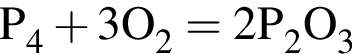
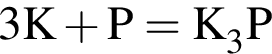
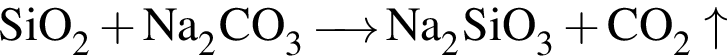 .
.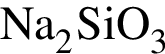 , В —
, В — 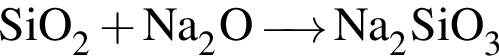
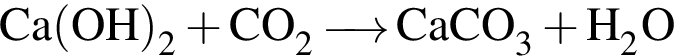 .
. 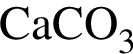
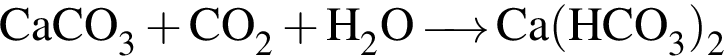 .
.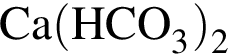
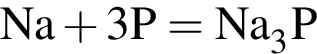
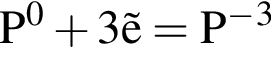 - окислитель
- окислитель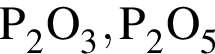 .
.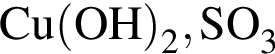
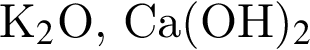
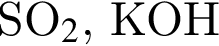
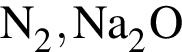
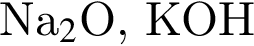
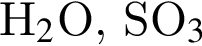
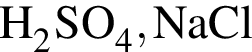
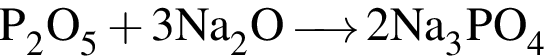 .
.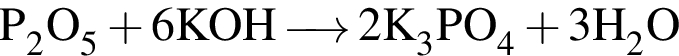 .
.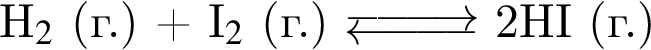 :
: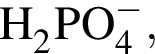
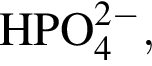
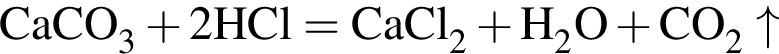
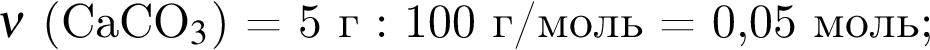
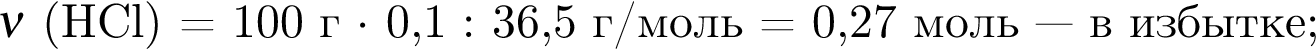
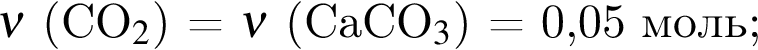
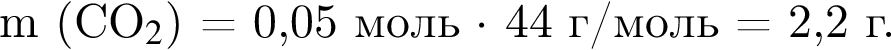
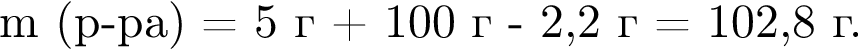
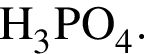 Массовая доля кислорода составляет:
Массовая доля кислорода составляет: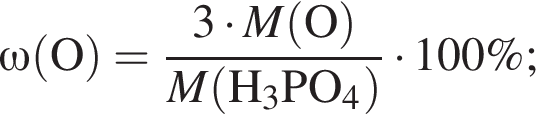
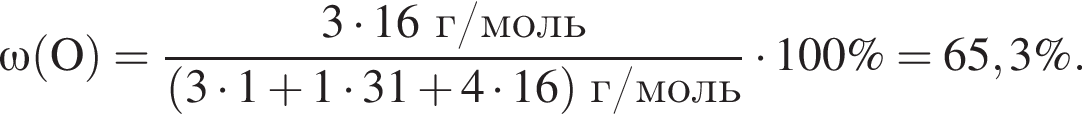
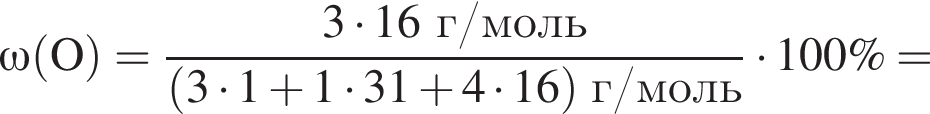
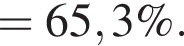


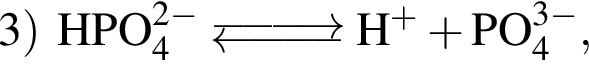
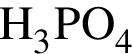 — кислота, поэтому взаимодействует с основными оксидами (
— кислота, поэтому взаимодействует с основными оксидами (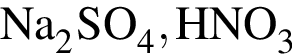
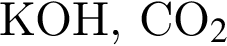
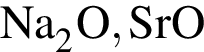
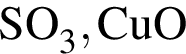
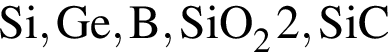 (карборунд),
(карборунд), 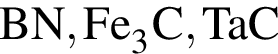 , красный и чёрный фосфор. В эту группу входят вещества, как правило, твёрдые и тугоплавкие вещества.
, красный и чёрный фосфор. В эту группу входят вещества, как правило, твёрдые и тугоплавкие вещества.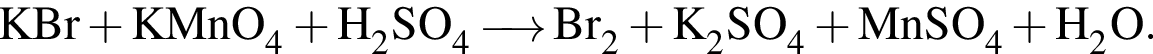
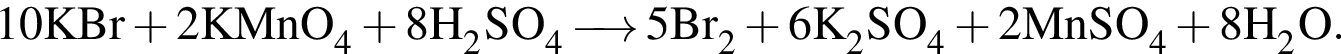
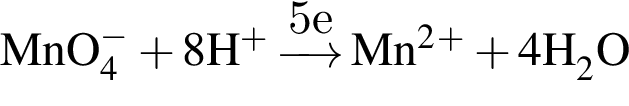
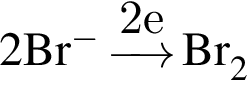
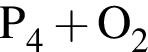 →
→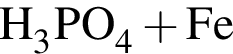 →
→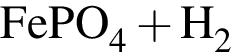
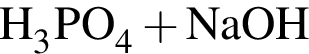 →
→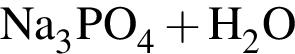
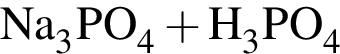 →
→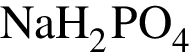 М=120
М=120

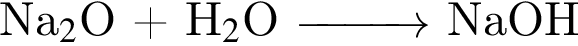

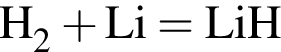 , водород понижает степень окисления с 0 до -1, т. е. принимает электроны и является окислителем.
, водород понижает степень окисления с 0 до -1, т. е. принимает электроны и является окислителем. 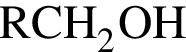 )=n(Cu)=32/64=0.5 моль
)=n(Cu)=32/64=0.5 моль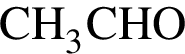 )=0.5*44=22 г
)=0.5*44=22 г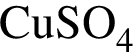 и 1 моль
и 1 моль 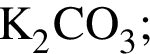

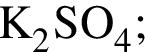
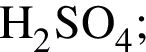
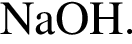
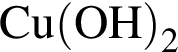 количеством 0,5 моль:
количеством 0,5 моль: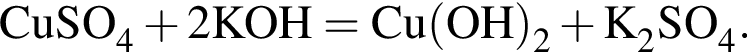
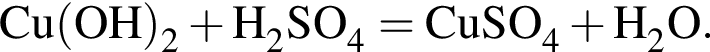
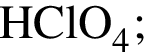
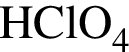 равна +7;
равна +7;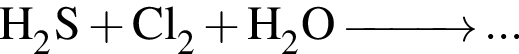 верными являются схемы перехода электронов:
верными являются схемы перехода электронов: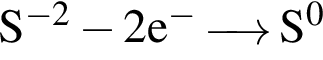
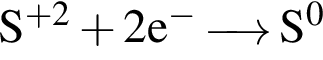
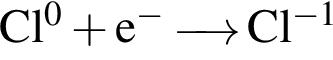
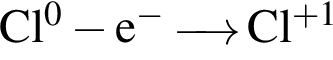
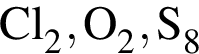 являются молекулами, а не символами. Символы химических элементов представлены в таблице Менделеева.
являются молекулами, а не символами. Символы химических элементов представлены в таблице Менделеева.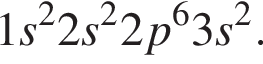 Число энергетических уровней, занятых электронами в атоме, равно:
Число энергетических уровней, занятых электронами в атоме, равно: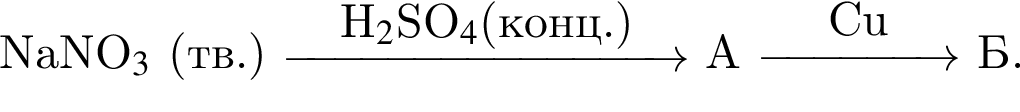
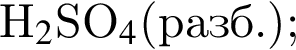
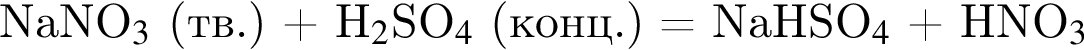
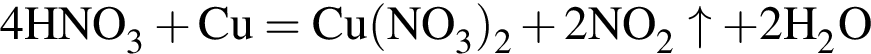
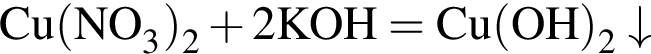
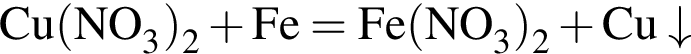
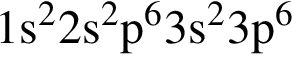 соответствует иону или атому в основном состоянии:
соответствует иону или атому в основном состоянии: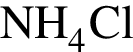 валентность азота равна IV, а степень окисления -3;
валентность азота равна IV, а степень окисления -3;